作為長期深耕該領域的CRO,向外,我們期待中國企業在全球競爭中嶄露頭角,打破復雜制劑進口壟斷;向內,我們希望與行業所有的參與者一起,找到應對競爭的航向與路徑。
做行業的“記錄者”與“同行者”,我們以數據為錨點,聚焦經皮領域藥物研發及審評動態的持續追蹤和分享,為行業與合作伙伴提供參考。
2025年3-4月核心數據速遞
審評數據:創新持續升溫
CDE受理經皮給藥上市申請53個,軟膏劑最多,幾乎全部為3類/4類仿制藥。
CDE批準44項臨床試驗,其中化藥1類創新藥9個(涉及4個品種),中藥1.1類2個;化藥2類改良藥11個,包括全國首個治療黃褐斑的凝膠貼膏KEM2111。
過評數據:中藥貼膏出現,熱門品種競爭加劇
一致性評價:共有38個產品過評,外用液體劑為主。
中藥貼膏:健民集團的中藥創新藥小兒牛黃退熱貼膏獲批,是2019年以來唯一一個獲批的1.1類中藥貼膏。
熱門品種:洛索洛芬鈉凝膠貼膏過評企業已滿7家,達到集采門檻;卡泊三醇倍他米松軟膏首仿上市。
一、上市審評動態
上市申請數據:


獲批數據:


重點品種上市情況:
洛索洛芬鈉凝膠貼膏,新增湖南普道醫藥、武漢法瑪星制藥、哈爾濱力強藥業3家獲批,3-4月有湖北民康藥業、浙江高跖醫藥2家企業在進行上市申報。洛索洛芬鈉凝膠貼膏的市場競爭已經進入“白熱化”。目前過評企業已滿7家,達到了集采門檻。
氟比洛芬凝膠貼膏,3-4月無新增獲批,但新增申報企業數最多(浙江高跖醫藥、河北鼎泰制藥、湖南金圃醫藥、河南羚銳制藥、杭州泓友醫藥等5家)。目前持證企業仍然只有2家(僅1家過評)。
卡泊三醇倍他米松軟膏,重慶華邦制藥首家獲批(視同過評),打破了原研藥“得膚寶”在國內將近17年的市場壟斷。
中藥經皮領域——小兒牛黃退熱貼膏,是2019年以來唯一一個獲批的1.1類中藥貼膏,由深耕兒藥領域的健民集團研發上市。藥品處方源自全國名中醫的臨床經驗方,填補了國內兒童退熱貼膏劑的空白。
2個熱門品種:米諾地爾搽劑/溶液、利丙雙卡因乳膏,米諾地爾搽劑/溶液有18個受理號獲批(涉及11家企業),利丙雙卡因乳膏則新增了5家上市企業。
臨床審評動態
臨床申請數據:


從劑型來看,凝膠劑6個,貼膏貼劑和外用液體分別5個,數量差異較小。從注冊類型看,1類創新藥共6個受理號,涉及3個產品(江蘇康緣藥業的KYS2301凝膠、江蘇普萊醫藥的抗菌肽PL-3301口腔凝膠、南京韋爾優眾醫藥的WEYZ-1乳膏),2類改良型新藥1個(上海澤德曼的TAP-1503乳膏),3/4類共10個受理號。
從企業分布來看,深圳琺瑪易的受理號與受理品種最多,共有4個受理號,涉及4個品種。其余10家企業均為1個品種。
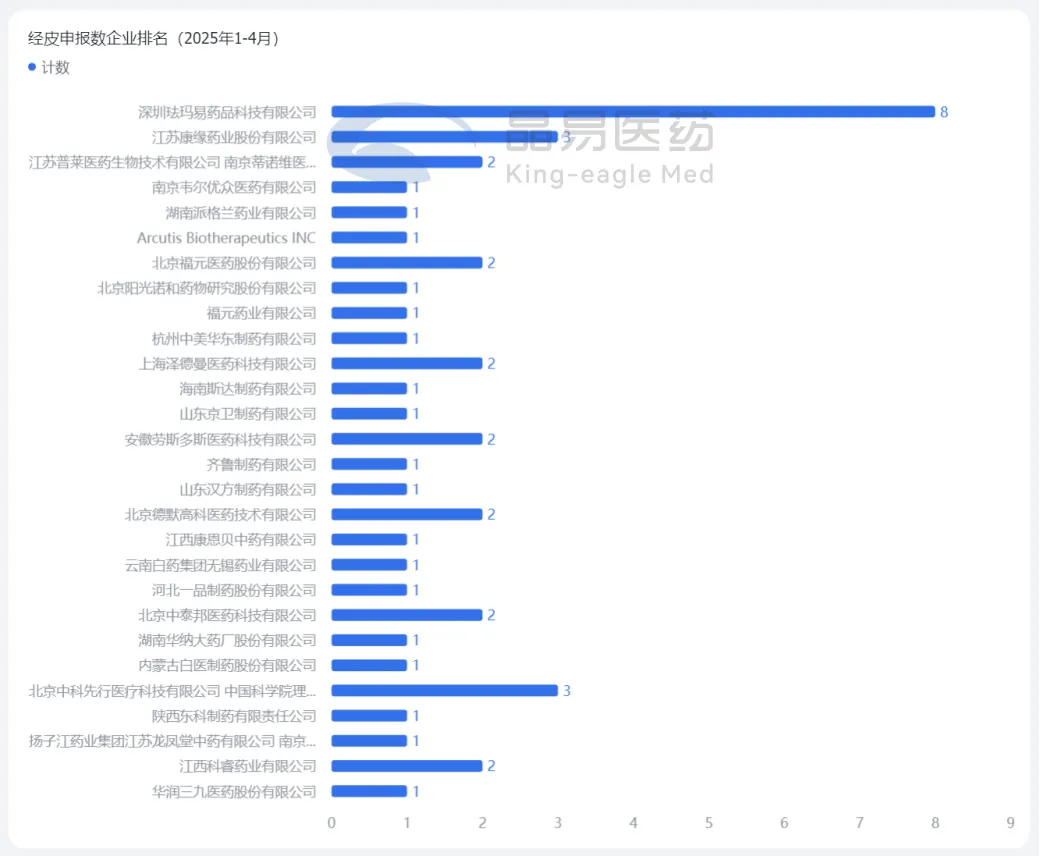
臨床批準數據:


從企業分布來看,深圳琺瑪易為批準臨床最多的企業,共8個受理號,涉及6個品種。其中包括1個2類改良型新藥KEM2111凝膠貼膏,這是全國首個治療黃褐斑的凝膠貼膏。
臨床登記備案數據:


唯一一個新型中藥貼劑類產品,通化萬通藥業的2.1類改良藥萬通筋骨巴布膏,此次為2024年上市申請被駁回后,再次申請開展Ⅲ期臨床。
貼膏貼劑市場格局
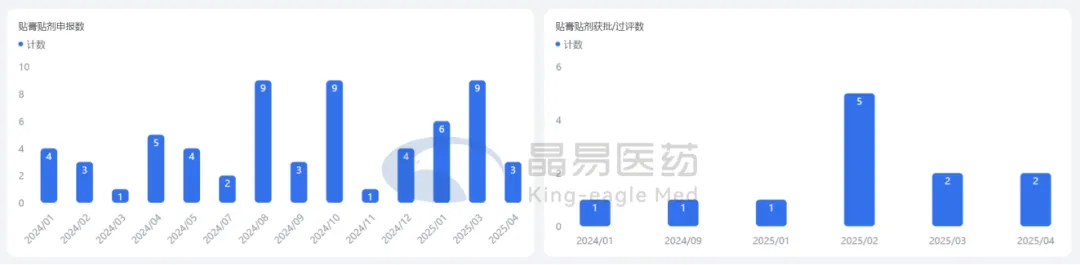
2024年以來,貼膏貼劑月度申報數均不超過10個。自2025年年初蘇州樂明藥業的洛索洛芬鈉凝膠貼膏獲批后,凝膠貼膏類產品的審批通道雖正式開啟,部分熱門品種競爭在加劇,但該類產品還未迎來明顯的增長點,新品種仍有較大空間。
新型中藥貼劑實現突破:
健民藥業的小兒牛黃退熱貼膏的上市,實現了2019年以來1類中藥貼劑的零突破,新型中藥貼劑市場開口。目前有江蘇康緣藥業的梔黃貼膏和海南賽立克藥業的馬錢子堿凝膠貼膏處于臨床階段。
憑借更低刺激性和致敏性、更高藥物滲透性、更廣泛適應癥,新型中藥貼劑更適用于我國越來越多的老年和兒童人群。國務院于2025年3月出臺《關于提升中藥質量促進中醫藥產業高質量發展的意見》,立足中藥全產業鏈布局,提出“加快構建現代化產業體系”的要求。中藥創新和現代化受到政策傾斜,新型中藥貼劑迎來機遇。


